Liberación de control J. 2024 noviembre: 375: 74-89. doi: 10.1016/j.jconrel.2024.08.049. Publicación electrónica del 5 de septiembre de 2024.
Optimización de un conector PEGilado en forma de colgante para conjugados anticuerpo-fármaco
Resumen
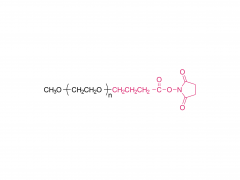
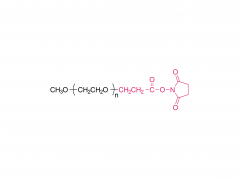
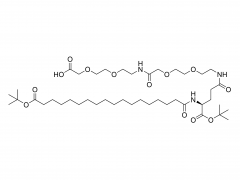
En este trabajo, concebimos y desarrollamos conjugados anticuerpo-fármaco (ADC) que podrían liberar eficazmente el fármaco después de la escisión enzimática del resto conector mediante proteasas tumorales. Los enlazadores anticuerpo-fármaco que utilizamos son el resultado de una optimización racional de un enlazador PEGilado previamente informado, PUREBRIGHT® MA-P12-PS, que mostró excelentes capacidades de carga de fármaco pero carecía de un mecanismo de descarga de fármaco incorporado, lo que limitaba la potencia del producto resultante. ADC. Para abordar esta limitación, optamos por incorporar un disparador sensible a proteasas en el enlazador para favorecer la liberación de un fármaco "sin PEG" en el interior de las células tumorales y, por tanto, obtener ADC potentes. Actualmente, la mayoría de los ADC comercializados se basan en el dipéptido Val-Cit seguido de un espaciador autoinmolable para liberar el fármaco en su forma no modificada. Aquí, seleccionamos dos secuencias peptídicas no tradicionales, un dipéptido Phe-Gly y un tripéptido Val-Ala-Gly y colocamos una u otra entre el fármaco en un lado (extremo N) y el resto del conector, incluido el PEG. resto, en el otro lado (extremo C), sin un grupo autoinmolador. Descubrimos que ambos conectores respondieron a la catepsina B, una enzima lisosomal de referencia, y liberaron un catabolito farmacológico libre de PEG, como se deseaba. Luego utilizamos los dos enlazadores para generar ADC basados en trastuzumab (un anticuerpo dirigido a HER2) y DM1 (un agente citotóxico dirigido a microtúbulos) con una relación fármaco-anticuerpo (DAR) promedio de 4 u 8. Los ADC mostraron restauración citotoxicidad in vitro, que fue proporcional a la carga de DM1 y generalmente mayor para los ADC que llevan Val-Ala-Gly en su estructura. En un modelo de ratón con cáncer de ovario, el ADC DAR 8 basado en Val-Ala-Gly se comportó mejor que Kadcyla® (un ADC aprobado de DAR 3.5 utilizado como control a lo largo de este estudio), lo que condujo a una mayor reducción del volumen del tumor y una supervivencia media más prolongada. . En conjunto, nuestros resultados representan un proceso exitoso de optimización del enlazador y alientan la aplicación del tripéptido Val-Ala-Gly como una alternativa a otros activadores de ADC sensibles a proteasas existentes.
Palabras clave: Conjugado anticuerpo-fármaco; Terapia anticancerígena; Enlazador peptídico escindible; Entrega de medicamentos; Mejoramiento; PEG.
Para obtener más información sobre el producto, contáctenos en:
Tel. de EE. UU.: 1-844-782-5734
Tel. de EE. UU.: 1-844-QUAL-PEG
CHN Tel: 400-918-9898
Correo electrónico: sales@sinopeg.com