En el campo de la biomedicina, la terapia CAR-T está experimentando un salto revolucionario, pasando de la preparación in vitro a la programación in vivo. El año 2025 marca un punto de inflexión crucial en el desarrollo de la terapia CAR-T in vivo. En junio, Capstan anunció que su terapia CAR-T in vivo CPTX2309, basada en el vector tLNP, había entrado oficialmente en ensayos clínicos de fase I. Posteriormente, AbbVie adquirió Capstan por 2100 millones de dólares en efectivo, obteniendo su tecnología patentada de plataforma tLNP. Esta transacción demuestra el gran reconocimiento de la terapia CAR-T in vivo por parte de las principales compañías farmacéuticas y marca la transición oficial de esta tecnología desde la fase de prueba de concepto a una nueva etapa de desarrollo clínico.
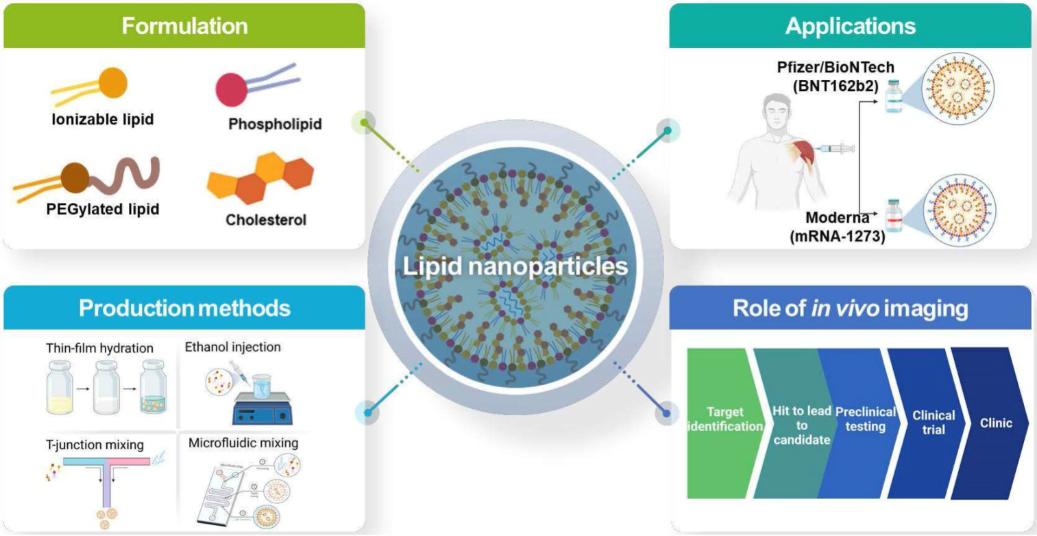
CAR-T y tLNP in vivo: la próxima tendencia en medicina de precisión
Antecedentes de la industria: Un salto revolucionario del in vitro al in vivo
La terapia CAR-T tradicional in vitro ha logrado avances notables en la leucemia y el linfoma de células B, pero su complejo proceso de fabricación, su elevado coste y su toxicidad han obstaculizado su popularización a gran escala. Según estudios del sector, el precio de un producto CAR-T comercial puede alcanzar entre 370.000 y 470.000 dólares estadounidenses, y el tiempo transcurrido desde la recolección de células hasta la reinfusión es de 3 a 5 semanas. Algunos pacientes no pueden esperar debido a la rápida progresión de su enfermedad.
La terapia CAR-T in vivo, con un enfoque tecnológico revolucionario, administra directamente los genes CAR al organismo mediante vectores especiales, evitando los engorrosos pasos in vitro y completando la "actualización del equipo" de las células T directamente en el cuerpo del paciente. Este modelo de "fábrica intracorporal" no solo simplifica significativamente el proceso de tratamiento, sino que también se espera que reduzca el coste a una décima parte del de la terapia CAR-T tradicional, convirtiéndose en un hito para la próxima generación de inmunoterapia celular.
tLNP: El sistema de administración central para CAR-T in vivo
En el camino de implementación de la terapia CAR-T in vivo, las nanopartículas lipídicas dirigidas (tLNP) se han convertido en la ruta técnica principal en la industria. Las tLNP otorgan a las LNP tradicionales la capacidad de reconocer y entregar con precisión la carga genética a las células T modificando su superficie con ligandos específicos (como anticuerpos y péptidos).
La tecnología principal consiste en acoplar con precisión el anticuerpo diana a la superficie del LNP para formar un sistema de administración similar a un misil de navegación. Cuando el tLNP penetra en el organismo, el ligando diana en la superficie guía a toda la nanopartícula para que se una específicamente a los linfocitos T y libera el ARNm-CAR en las células mediante endocitosis, logrando así la reprogramación in situ de los linfocitos T.
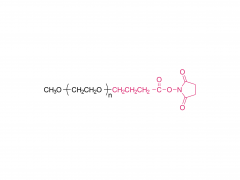
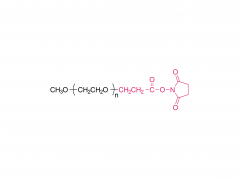
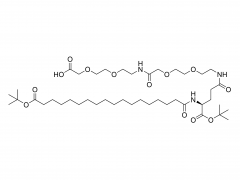
DSPE-PEG-MAL
El "puente químico" clave para la construcción de tLNP
Impulsando la entrega dirigida: Triple potenciación de la funcionalización de tLNP
En el complejo sistema de construcción de tLNP, DSPE-PEG-MAL desempeña un papel dinámico de "ejecutor". Su diseño estructural se corresponde con precisión con sus funciones clave en el proceso de preparación, y su función puede descomponerse en los siguientes tres pasos progresivos y coherentes.
· Incrustaciones y anclajes: posicionamiento preciso desde la fase de solución hasta la fase de membrana
Durante el proceso de autoensamblaje del LNP, DSPE-PEG-MAL puede anclarse espontáneamente a la membrana de la bicapa lipídica en formación gracias a las propiedades fisicoquímicas de su cola hidrófoba de DSPE. Este proceso garantiza que toda la molécula se integre en la estructura del LNP con una orientación predefinida y de forma estable, sentando las bases para funciones posteriores.
· Estiramiento y Protección: Establecer líneas de defensa espaciales en la interfaz
Una vez ancladas, las cadenas hidrófilas de PEG2000 se extienden completamente en el entorno acuoso que rodea la LNP, formando una capa protectora flexible e hidratada, similar a un cepillo. Esta capa protectora actúa como la primera línea de defensa de la LNP, manteniendo su estabilidad fisicoquímica e integridad funcional en el complejo entorno in vivo, inhibiendo la adsorción de proteínas inespecíficas y reduciendo la agregación de partículas, prolongando así su vida media circulante en el organismo.
· Clic y empoderamiento: La transformación química de los portaaviones generales a los misiles de precisión
El grupo maleimida (-MAL), ubicado al final de la cadena de PEG, es el interruptor químico que dota a las LNP de inteligencia. Al ser un sitio de bioacoplamiento altamente selectivo, puede reaccionar eficientemente con los grupos tiol de los anticuerpos modificados (por ejemplo, introducidos mediante la reducción de enlaces disulfuro o utilizando reactivos como SATA). Es precisamente mediante este paso de conexión covalente irreversible que las LNPS ordinarias se potencian y evolucionan a TLNPS dirigidas, capaces de reconocer con precisión antígenos específicos de la superficie celular.
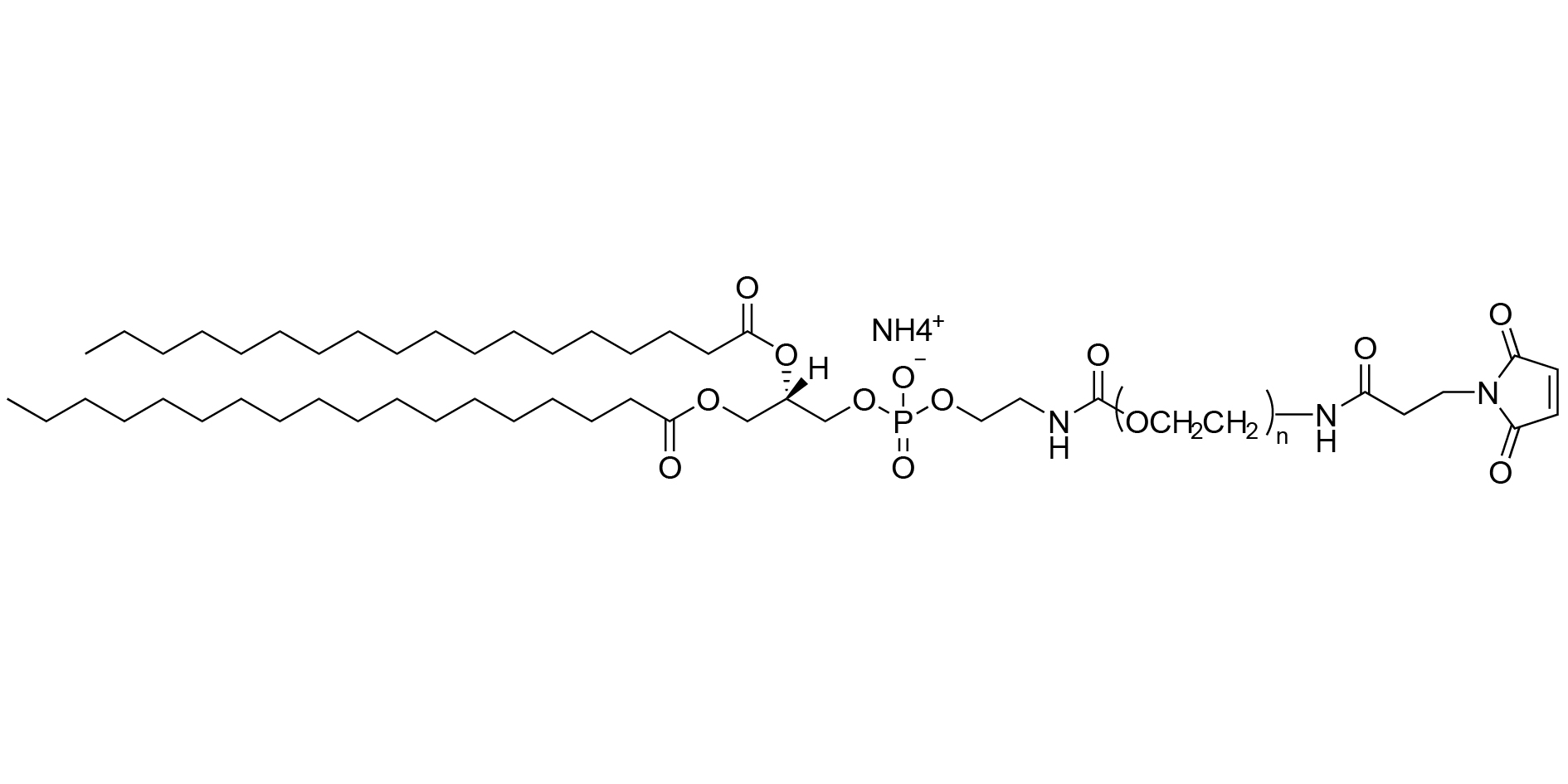
Figura 1: Diagrama esquemático de la estructura molecular de DSPE-PEG-MAL (sal de amonio)
El enfoque técnico para lograr la conjugación de anticuerpos en la superficie de LNP
El uso de DSPE-PEG-MAL para lograr la conjugación de anticuerpos en la superficie de LNP es actualmente la estrategia más desarrollada y ampliamente aplicada para la construcción de tLNP. Este proceso suele implicar tres enlaces principales:
Preparación de LNP: El DSPE-PEG-MAL se mezcla con otros componentes lipídicos (lípidos ionizables, lípidos auxiliares, colesterol, lípidos de PEG) mediante tecnología de mezcla microfluídica para preparar el LNP. En este punto, el grupo maleimida (-MAL) del DSPE-PEG-MAL queda expuesto en la superficie del LNP.
2. Pretratamiento con anticuerpos: De acuerdo con los métodos comunes para construir LNPS dirigidos en la industria (como los descritos por Capstan Therapeutics en la patente WO2024249954), los anticuerpos se modifican con tiol (-SH) para prepararlos para la reacción de acoplamiento posterior.
3. Reacción de acoplamiento: El anticuerpo conjugado con tiol (-SH) se incuba con LNP en un tampón adecuado (como PBS, pH 7,4) a baja temperatura (por ejemplo, 4 °C) (generalmente durante varias horas o toda la noche). Los grupos tiol del anticuerpo se unen covalentemente a los grupos maleimida (-MAL) de la superficie de la LNP, completando así la modificación de funcionalización deseada.
En comparación con vectores virales como lentivirus y virus adenoasociados, el sistema de administración de LNP basado en DSPE-PEG-MAL tiene ventajas como baja inmunogenicidad, ningún riesgo de mutación por inserción y fácil producción a gran escala, lo que lo convierte en un vector ideal para CAR-T in vivo.
Las principales ventajas del DSPE-PEG-MAL de grado GMP de SINOPEG
Producción a nivel GMP y suministro inmediato
En la actual ola de I+D de CAR-T in vivo, el suministro estable y de alta calidad de excipientes clave es fundamental para garantizar el buen desarrollo de la I+D. Xiamen SINOPEGe ha establecido un sistema completo de gestión de calidad según las BPF, ha logrado la producción a gran escala de DSPE-PEG-MAL conforme a las BPF y ha acumulado un inventario de reserva suficiente.
La presentación dual para CDE y DMF está a punto de completarse
Para ayudar mejor a los clientes en las solicitudes de registro de medicamentos, nuestro producto DSPE-PEG-MAL se está promocionando activamente:
· Registro y presentación de excipientes CDE de China: una vez completado, se puede asociar directamente para solicitudes de registro de medicamentos.
· Presentación de DMF ante la FDA en los Estados Unidos: proporciona una base autorizada para demostrar la calidad y el cumplimiento de los excipientes ante la FDA.
SINOPEG ha establecido un sistema integral de control de calidad, desde la obtención de materias primas y los procesos de síntesis hasta el control de purificación. Somos conscientes de que, en terapias de vanguardia como las CAR-T in vivo, cualquier pequeña diferencia en los excipientes puede tener un gran impacto en las propiedades fisicoquímicas, el comportamiento in vivo e incluso el efecto terapéutico de la formulación final. No solo controlamos estrictamente la pureza, la actividad del grupo maleimida (-MAL) y la integridad de la cadena de PEG, sino que, gracias a nuestro profundo conocimiento de la producción industrial de PEG y sus derivados activos a lo largo de los años y a nuestra experiencia en la solicitud de múltiples proyectos IND, hemos desarrollado una serie de pruebas de caracterización específicas. Las ventajas diferenciadoras que ofrecen estas caracterizaciones fisicoquímicas exhaustivas permiten obtener un respaldo de datos más completo para la solicitud de su proyecto. Tras completar la doble solicitud, los clientes pueden utilizar directamente nuestro número de solicitud, lo que simplifica considerablemente el proceso de solicitud de IND (Solicitud de Ensayo Clínico de Nuevo Fármaco) o NDA (Solicitud de Comercialización de Nuevo Fármaco), ahorra tiempo y costes laborales, y mejora significativamente la tasa de éxito de las solicitudes.
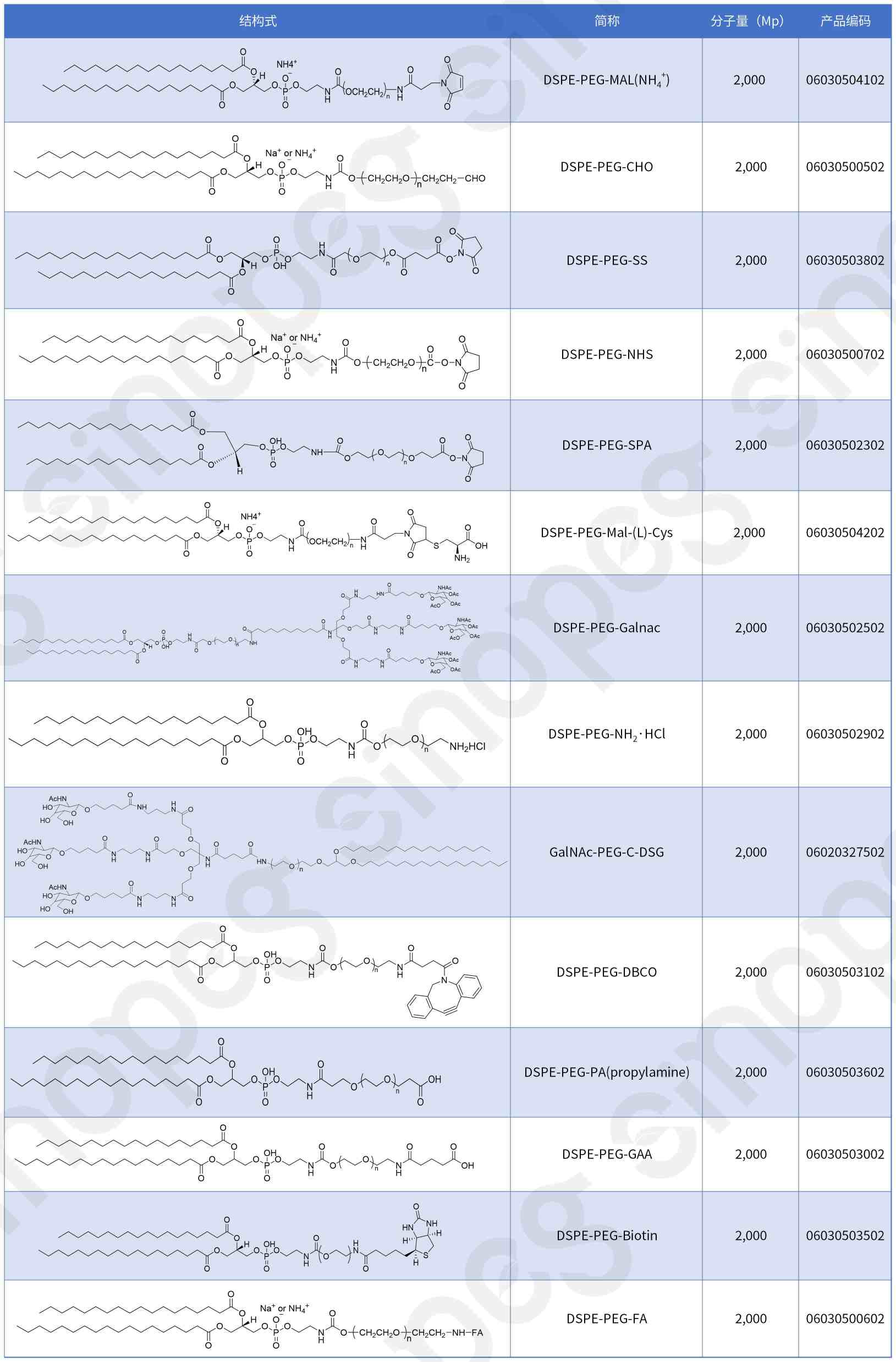
Ampliación de los productos de la serie DSPE-PEG
Además de DSPE-PEG-MAL, nuestra empresa también puede proporcionar servicios de desarrollo personalizados para una variedad de derivados de fosfolípidos-PEG funcionalizados para satisfacer diferentes necesidades de I+D.
Referencia:
1. Capstan Therapeutics. Capstan Therapeutics anuncia el inicio del ensayo de fase 1 de la terapia CAR-T in vivo líder, CPTX2309, para el tratamiento de enfermedades autoinmunes. Business Wire. 11 de junio de 2025.
2. AbbVie. AbbVie adquirirá Capstan Therapeutics, reforzando aún más su compromiso de transformar la atención al paciente en inmunología. Centro de Noticias de AbbVie. 30 de junio de 2025.
3. Sociedad Americana de Oncología Clínica. Terapia con células CAR-T: Costos y consideraciones. Actas de la Reunión Anual de la ASCO. 2024.
4. Smith J, et al. Las células CAR-T in vivo demuestran una potente actividad antitumoral con una menor complejidad de fabricación. Nature Biotechnology. 2023;41(5):678-685.
5. Wang D, et al. Nanopartículas lipídicas dirigidas para la ingeniería de células T in vivo. Science Advances. 2024;10(12):eadl2165.
6. Chen X, et al. LNP conjugado con anticuerpos para la administración precisa de genes in vivo a células T. Cell Reports Medicine. 2024;5(3):101489.
7. Zhang Y, et al. Estructura molecular y propiedades de anclaje a la membrana de los lípidos DSPE-PEG. Biochimica et Biophysica Acta. 2023;1865(4):184321.
8. Gabizon A, et al. Prolongación del tiempo de circulación y aumento de la acumulación de doxorrubicina en exudados malignos encapsulada en liposomas recubiertos de polietilenglicol. Cancer Research. 1994;54:987-992.
9. Hermanson GT. Técnicas de bioconjugados. 3.ª ed. Academic Press; 2021.
10. Wei X, et al. Síntesis microfluídica de nanopartículas lipídicas específicas para la ingeniería de células T. Lab on a Chip. 2024;24(8):2156-2168.
11. Kato T, et al. Conjugación eficiente de anticuerpos mediante el reactivo de Traut para la funcionalización de LNP. Química de Bioconjugados. 2023;34(7):1256-1265.
12. Li M, et al. Conjugación covalente de anticuerpos contra la superficie de LNP para administración dirigida. Revista de Liberación Controlada. 2024;368:456-467.
13. Xu Q, et al. Sistemas de administración no viral para la ingeniería de células CAR-T in vivo. Nature Reviews Materials. 2024;9(3):189-205.