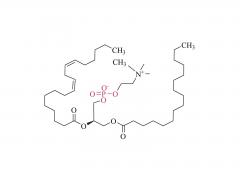
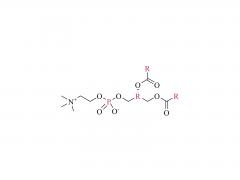
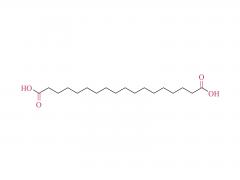
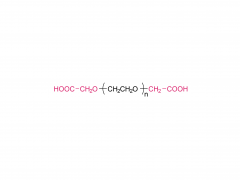
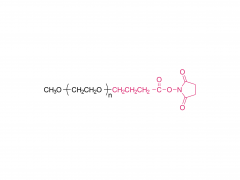
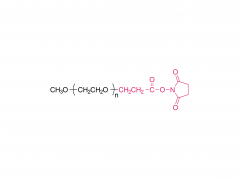
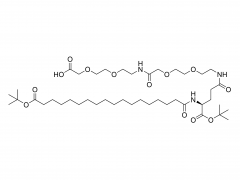
Farmacia. 2 de agosto de 2022; 14 (8): 1614. doi: 10.3390/farmacéutica14081614. La longitud del espaciador de PEG afecta sustancialmente la orientación de los nanoportadores basados en anticuerpos en subconjuntos de células dendríticas Resumen El éxito de la orientación celular depende del posicionamiento controlado de anticuerpos específicos del tipo de célula en la superficie del nanoportador (NC). La inmovilización incontrolada de anticuerpos da como resultado una captación celular no deseada debido a la interacción celular mediada por Fc. En consecuencia, se necesita una inmovilización precisa de la región Fc hacia la superficie del nanoportador, manteniendo las regiones Fab libremente accesibles para la unión al antígeno. Además, el anticuerpo debe estar a cierta distancia de la superficie del nanoportador, lo que influye en el rendimiento de la orientación después de la formación de la corona biomolecular. Esto se puede lograr utilizando moléculas enlazadoras de PEG. Aquí demostramos la orientación específica del tipo de célula para las células dendríticas (DC) como reguladores celulares clave de las respuestas inmunes. Sin embargo, hasta la fecha, aún es necesario realizar experimentos dirigidos a células dendríticas utilizando diferentes longitudes de conector. En consecuencia, nos centramos en la modificación de la superficie de nanoportadores con conectores PEG de diferentes pesos moleculares (0,65, 2 y 5 kDa) y su capacidad para reducir la captación celular no deseada, al mismo tiempo que logramos una focalización eficiente en DC a través de anticuerpos inmovilizados covalentemente (orientación sigilosa). Nuestros hallazgos demuestran que la longitud del conector PEG afecta significativamente la orientación de las células dendríticas activas desde líneas celulares (DC2.4) a células primarias (BMDC, DC esplenocíticas convencionales tipo 1 (cDC1)). Si bien los nanoportadores funcionalizados con anticuerpos con una longitud de PEG más corta (0,65 kDa) mostraron la mejor orientación en DC2.4, se requirió una longitud de PEG más larga (5 kDa) para acumularse específicamente en BMDC y cDC1 esplenocítica. Nuestro estudio destaca que estos aspectos cruciales deben tenerse en cuenta al abordar subconjuntos de células dendríticas, que son de gran importancia en los campos de la inmunoterapia contra el cáncer y el desarrollo de vacunas. Palabras clave: PEG; funcionalización de anticuerpos; focalización en células dendríticas; nanopartículas; nanovacuna. Para obtener más información sobre el producto, contáctenos en: Tel. de EE. UU.: 1-844-782-5734 Tel. de EE. UU.: 1-844-QUAL-PEG CHN Tel: 400-918-9898 Correo electrónico: sales@sinopeg.com
ver más