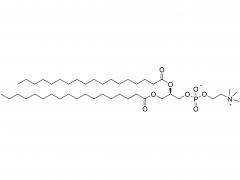
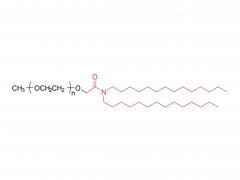
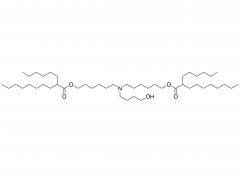
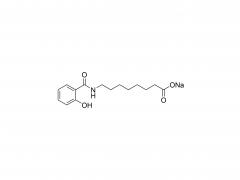
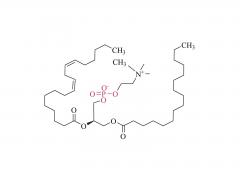
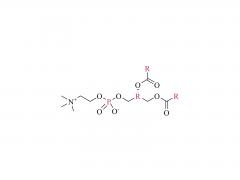
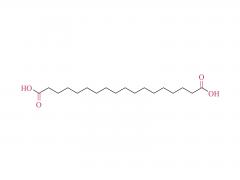
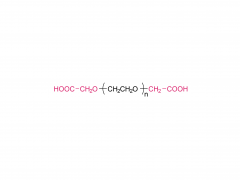
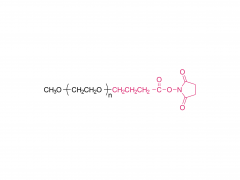
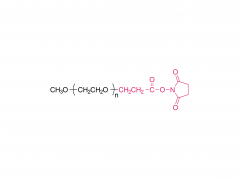
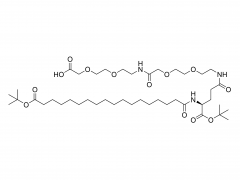
Química bioconjugada. 21 de julio de 2021; 32 (7): 1263-1275. doi: 10.1021/acs.bioconjchem.1c00172. Publicación electrónica 2021 30 de mayo. La influencia de un conector de polietilenglicol en el metabolismo y la farmacocinética de un anticuerpo radiomarcado con 89Zr Resumen La mayor parte del trabajo experimental en el ámbito de la química de bioconjugación se centra en el uso de nuevos métodos para construir enlaces covalentes entre una molécula de carga y una proteína de interés, como un anticuerpo monoclonal (mAb). La formación de enlaces es importante para generar nuevas herramientas de diagnóstico, sin embargo, cuando estos compuestos avanzan a estudios preclínicos in vitro e in vivo, y luego para su traducción a la clínica, es importante comprender el destino de los metabolitos potenciales que surgen de la degradación química o enzimática de la construcción. para obtener una imagen completa del rendimiento farmacocinético de un nuevo compuesto. En el contexto del diseño de nuevos métodos bioconjugados para marcar anticuerpos con el radionúclido emisor de positrones 89Zr, previamente desarrollamos un proceso fotoquímico para producir 89Zr-mAb. Los estudios experimentales sobre construcciones de mAb [89Zr]ZrDFO-PEG3-azepin revelaron que la incorporación del conector tris-polietilenglicol (PEG3) mejoraba la solubilidad de la fase acuosa y la conversión radioquímica. Sin embargo, el uso de un conector PEG3 también tiene un impacto en el tiempo de residencia de la construcción en todo el cuerpo, lo que lleva a una excreción más rápida de la actividad 89Zr en comparación con los radiotrazadores que carecen de la cadena PEG3. En este trabajo, investigamos el destino metabólico de ocho posibles metabolitos que surgen de la desconexión lógica de [89Zr]ZrDFO-PEG3-azepin-mAb en enlaces que son susceptibles a la escisión química o enzimática. Se informa la síntesis combinada con radiomarcaje con 89Zr, imágenes de tomografía por emisión de positrones de animales pequeños en múltiples puntos de tiempo de 0 a 20 h, y mediciones de la vida media efectiva para la excreción en todo el cuerpo. Las conclusiones son que el uso de un conector PEG3 no es inocente en términos de su impacto en la mejora del metabolismo de los mAb [89Zr]ZrDFO-PEG3-azepin. En la mayoría de los casos, la degradación puede producir metabolitos que se eliminan rápidamente del cuerpo, mejorando así el contraste de la imagen al reducir la acumulación inespecífica y la retención de 89Zr en órganos subyacentes como el hígado, el bazo, los riñones y los huesos. Para obtener más información sobre el producto, contáctenos en: Tel. de EE. UU.: 1-844-782-5734 Tel. de EE. UU.: 1-844-QUAL-PEG Teléfono CHN: 400-918-9898 Correo electrónico: sales@sinopeg.com
ver más