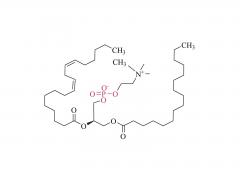
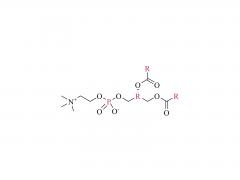
J Virol. 13 de junio de 2024;98(6):e0057824. doi: 10.1128/jvi.00578-24. Publicación electrónica 2024 20 de mayo. Una vacuna contra el virus de Lassa basada en ARNm-LNP induce inmunidad protectora en ratones Abstracto El virus Lassa del mammarenavirus (LASV) causa la fiebre hemorrágica potencialmente mortal, la fiebre de Lassa. La falta de contramedidas médicas autorizadas contra el LASV subraya la urgente necesidad de desarrollar nuevas vacunas LASV, que se ha visto obstaculizada por el requisito de una instalación de nivel de bioseguridad 4 para manipular LASV vivo. Aquí, investigamos la eficacia de las vacunas basadas en nanopartículas lipídicas de ARNm (ARNm-LNP) que expresan el precursor de la glucoproteína LASV (LASgpc) o la nucleoproteína (LCMnp) del mammarenavirus prototípico, el virus de la coriomeningitis linfocítica (LCMV), en ratones. Dos dosis de LASgpc o LCMnp-ARNm-LNP administradas por vía intravenosa (iv) protegieron a ratones C57BL/6 de un desafío letal con un LCMV recombinante (r) que expresa un LASgpc modificado (rLCMV/LASgpc2m) inoculado intracranealmente. La inmunización intramuscular (im) con dos dosis de LASgpc- o LCMnp-ARNm-LNP redujo significativamente la carga viral en ratones C57BL/6 inoculados iv con rLCMV/LASgpc2m. Se observaron altos niveles de viremia y letalidad en ratones CBA inoculados iv con rLCMV/LASgpc2m, que fueron anulados por la inmunización im con dos dosis de LASgpc-ARNm-LNP. La eficacia protectora de dos dosis im de LCMnp-ARNm-LNP se confirmó en un modelo de enfermedad hemorrágica letal de ratones FVB inoculados iv con rLCMV de tipo silvestre. En todas las condiciones probadas, se detectaron niveles insignificantes y altos de anticuerpos específicos contra LASgpc y LCMnp en ratones inmunizados con ARNm-LNP, respectivamente, pero se indujeron respuestas robustas de células T CD8+ específicas contra LASgpc y LCMnp. En consecuencia, el plasma de ratones inmunizados con LASgpc-ARNm-LNP no mostró actividad neutralizante. Nuestros hallazgos y los modelos murinos sustitutos de infección por LASV, que pueden estudiarse a un nivel de biocontención reducido, proporcionan una base fundamental para el rápido desarrollo de vacunas contra LASV basadas en ARNm-LNP. IMPORTANCIA: El virus de Lassa (LASV) es un mammarenavirus altamente patógeno responsable de cientos de miles de infecciones anuales en países de África Occidental, causando un alto número de casos letales de fiebre de Lassa (LF). A pesar de su significativo impacto en la salud humana, no existen contramedidas médicas clínicamente aprobadas, seguras y eficaces contra la LF. El requisito de una instalación de nivel de bioseguridad 4 para manipular LASV vivo ha sido uno de los principales obstáculos para la investigación y el desarrollo de contramedidas contra LASV. En este trabajo, informamos que dos dosis de vacunas basadas en nanopartículas lipídicas de ARNm que expresan el precursor de la glicoproteína LASV (LASgpc) o la nucleoproteína (LCMnp) del virus de ...
ver más